全球细胞与基因治疗(CGT)行业正经历从实验室研究向产业化落地的关键跃迁。据中研普华产业研究院预测,2026年全球CGT市场规模将突破800亿美元,2024-2030年复合增长率达47.2%。这一增长背后,是技术创新与资本投入的双重驱动。
一、技术创新:从“工具革命”到“系统整合”
1. 基因编辑技术:精准度与安全性的双重跃升
CRISPR-Cas9技术通过高保真变体(如iGeoCas9)将脱靶率降至0.1%以下,推动基因治疗从“高风险一次性治疗”向“可编程医疗平台”转型。例如,2026年全球首个针对苯丙酮尿症(PKU)的个体化CRISPR疗法进入III期临床,通过脂质纳米颗粒(LNP)递送系统实现体内直接编辑,避免传统体外细胞提取的侵入性操作。
碱基编辑(Base Editing)与先导编辑(Prime Editing)技术进一步拓展应用边界。前者通过单碱基替换修复基因突变,已用于治疗镰状细胞贫血;后者则实现任意DNA序列的精准插入或删除,为杜氏肌营养不良症等复杂疾病提供新解法。
2. 递送系统:非病毒载体与组织靶向性突破
递送技术是CGT临床转化的核心瓶颈。2026年,LNP递送系统在mRNA疫苗领域的成功经验加速向基因治疗迁移,全球在研LNP-CRISPR项目超50个,覆盖遗传病、肿瘤、感染性疾病等领域。外泌体(Exosome)递送技术凭借低免疫原性、高组织穿透性等优势,成为脑部疾病治疗的新突破口。例如,针对胶质母细胞瘤的外泌体-CRISPR疗法通过血脑屏障,实现肿瘤基因的精准敲除。
非病毒递送系统的崛起也推动行业成本下降。2026年,全球首款基于LNP的体内CAR-T疗法获批上市,治疗成本较传统自体CAR-T降低60%,标志着基因治疗从“天价疗法”向“可及创新”迈进。
3. 细胞治疗:从血液瘤到实体瘤的跨越
CAR-T疗法在血液肿瘤领域已实现高缓解率,但实体瘤治疗仍是行业痛点。2026年,双靶点CAR-T(如CD19/BCMA双靶点)与TCR-T疗法成为实体瘤治疗主流,全球在研项目超300个。例如,Adaptimmune Therapeutics的TCR-T疗法被批准用于治疗滑膜肉瘤,标志着细胞疗法在实体瘤中的应用进一步拓展。
通用型细胞治疗(UCAR-T)技术通过基因编辑敲除T细胞的HLA基因,降低免疫排斥风险,实现“现货型”产品供应。2027年,UCAR-T成本预计降至当前自体CAR-T的50%,覆盖30%血液瘤患者。
4. AI与合成生物学:重塑研发范式
AI技术贯穿CGT研发全链条:
靶点发现:生成式AI将周期从18个月缩短至3个月(如英伟达与礼来合作平台);
临床试验:AI通过真实世界数据(RWD)优化患者分层,将入组效率提升40%;
生产优化:数字孪生技术实现AAV载体生产的实时监控,将批次合格率从75%提升至92%。
合成生物学则通过构建“智能细胞”实现动态响应疾病信号。例如,针对肿瘤微环境的“逻辑门控”CAR-T细胞,仅在检测到双重肿瘤抗原时激活,显著降低脱靶毒性。
据中研普华产业研究院最新发布的《2026-2030年中国细胞与基因治疗(CGT)行业全景调研与发展趋势预测报告》预测分析
二、市场格局:区域竞争与产业链重构
1. 区域竞争:北美领跑,亚太突围
北美:占全球42.8%市场份额,FDA监管框架成熟,Thermo Fisher、Gilead等企业主导CDMO与工具试剂市场。2026年,辉瑞、默克等企业通过“资产置换+收益分成”模式锁定长期产能,例如药明生物与全球Top20药企签订10年期产能锁定协议。
欧洲:德国以28.5%份额领跑,英国通过“癌症药物基金”加速创新疗法覆盖。罗氏通过收购Intra-Cellular Therapies强化CNS药物管线,诺华则以120亿美元收购Avidity Biosciences布局核酸药物。
亚太:中国占比35.5%,NMPA审批周期压缩40%,上海、北京设立超200亿元专项产业基金。日本iPSC技术全球领先,印度CDMO成本优势吸引全球布局。
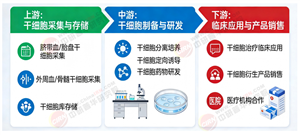
2. 产业链重构:从“单点突破”到“生态协同”
上游:核心原材料与设备国产化加速。依科赛生物等企业打破国外技术垄断,其CGT无血清培养基系列产品均已获得DMF认证,助力多家客户FDA与CDE中美IND申报成功。
中游:CDMO企业崛起。药明生物2025年CGT产能翻倍,承接超40%行业订单;复星凯特、传奇生物等企业通过“License-out+NewCo”模式实现管线全球化布局。
下游:支付体系与临床应用创新。上海试点“按疗效分期付款”模式,患者自付比例从80%降至40%;平安健康推出CGT专项保险,2027年覆盖用户超50万。
三、投资机会:技术差异化与商业化落地
1. 短期机会:聚焦技术成熟度与临床数据确定性
上游核心材料:关注国产替代能力强的试剂供应商(如菲鹏生物)和CDMO龙头(如药明生物)。2026年,全球CGT CDMO市场规模达1910亿美元,早期项目融资难度加大,但拥有先进临床试验和人类数据的“后期公司”仍受资本青睐。
肿瘤CGT:国内已有5款CAR-T产品上市,靶点以CD19、BCMA为主。2025年预计更多实体瘤疗法进入临床Ⅲ期,布局多靶点、实体瘤管线的企业(如科济药业、传奇生物)具备先发优势。
2. 长期机会:布局慢性病与国际化能力
慢性病基因修正:针对糖尿病、心血管疾病、帕金森病等慢性病的基因治疗研究已取得阶段性进展。例如,针对心血管疾病的PCSK9基因沉默疗法、针对帕金森病的神经营养因子基因疗法进入临床后期。
国际化布局:欧美企业占全球CAR-T市场80%份额,中国企业需通过技术差异化突围。例如,开发针对亚洲高发肿瘤(如胃癌、肝癌)的疗法,或通过与跨国药企合作加速全球化进程。
3. 风险对冲:关注政策导向与供应链安全
政策风险:中美欧对CGT产品的审批标准趋严,需关注监管科学进展(如长期随访标准建立、伦理审查强化)。
供应链风险:高端仪器(如超分辨显微镜)与特殊材料(如医用级AAV载体)仍依赖进口,国产化率不足30%。投资具备自主可控供应链的企业(如依科赛生物)可降低风险。
全球CGT行业正站在技术突破与产业升级的历史交汇点。未来五年,行业将呈现三大趋势:
技术融合:基因编辑、细胞治疗、AI、合成生物学深度交叉,催生新一代精准疗法;
应用拓展:从罕见病、血液肿瘤向常见病延伸,市场空间进一步打开;
生态竞争:企业需在技术平台、适应症选择、成本控制等维度建立优势,同时通过支付模式创新提升疗法可及性。
对于投资者而言,需平衡技术创新与商业化落地,抓住“治疗革命”中的结构性机会;对于企业而言,应以“技术为本、合规为基、生态为翼”构建核心竞争力,共同推动行业从“高值特供”向“普惠可及”的质变。
若您期望获取更多行业前沿资讯与专业研究成果,可查阅中研普华产业研究院最新推出的《2026-2030年中国细胞与基因治疗(CGT)行业全景调研与发展趋势预测报告》,此报告立足全球视角,结合本土实际,为企业制定战略布局提供权威参考。




















 研究院服务号
研究院服务号
 中研网订阅号
中研网订阅号