引言:生物医药——人类健康的守护者与未来产业的引擎
生物医药产业作为战略性新兴产业的核心领域,融合了生物学、医学、工程学等多学科前沿技术,已成为全球科技竞争的制高点和经济增长的新引擎。从基因编辑到细胞治疗,从精准医疗到AI制药,生物医药的每一次突破都在重塑人类对抗疾病的方式。截至2026年,随着全球人口老龄化加剧、健康需求升级以及技术革命的深度渗透,生物医药行业正经历前所未有的变革。
一、行业现状:技术驱动下的结构性变革
1. 技术突破:从“治疗”到“治愈”的跨越
基因与细胞治疗进入临床爆发期:CRISPR-Cas9基因编辑技术的安全性与精准度显著提升,已从单基因遗传病治疗拓展至癌症、感染性疾病等领域。CAR-T细胞疗法在血液肿瘤中的治愈率突破传统化疗瓶颈,实体瘤治疗成为下一阶段攻关重点。干细胞技术通过诱导多能干细胞(iPSC)实现规模化生产,为帕金森病、糖尿病等慢性病提供再生医学解决方案。
AI与生物技术深度融合:AlphaFold3等算法突破蛋白质结构预测难题,加速药物靶点发现;生成式AI设计新型小分子化合物,将传统药物研发周期从数年缩短至数月。AI辅助诊断系统通过多模态数据融合,实现癌症早期筛查准确率超90%,推动医疗资源下沉。
合成生物学重构产业逻辑:通过设计-构建-测试-学习(DBTL)循环,微生物细胞工厂高效合成青蒿素、胰岛素等复杂药物,成本降低;DNA存储技术突破容量极限,为生物数据长期保存提供新路径。
2. 产业生态:全球分工与区域竞争并存
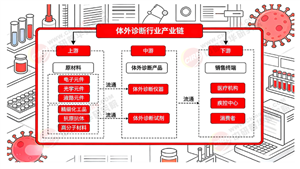
产业链分工细化:上游原料供应商通过生物催化技术实现酶制剂、培养基的绿色生产;中游CDMO企业依托模块化工厂满足个性化药物定制需求;下游医疗终端形成“医院-社区-家庭”三级服务网络,远程诊疗与智能设备普及率提升。
区域集群效应显著:美国波士顿-剑桥地区依托哈佛、MIT等高校形成“研发-转化-资本”闭环;中国长三角地区通过政策协同构建从基因测序到细胞治疗的全产业链;欧洲凭借严格的监管体系成为高端医疗器械创新高地。
跨界融合加速:科技巨头(如谷歌、华为)通过AI算法切入药物发现领域;传统药企(如罗氏、恒瑞)与生物技术公司(如Moderna、传奇生物)建立战略联盟,形成“大而全”与“小而美”共生格局。
3. 政策环境:监管科学引领创新合规
适应性监管框架建立:FDA推出“实时肿瘤审评”(RTOR)试点,将抗癌药审批时间压缩;中国NMPA实施药品上市许可持有人(MAH)制度,激发创新主体活力;欧盟《通用数据保护条例》(GDPR)细化生物数据使用边界,平衡隐私与创新。
伦理治理成为核心议题:基因编辑婴儿事件后,全球成立国际人类基因组编辑委员会(IHG-EC),制定《可遗传基因组编辑临床研究原则》;脑机接口技术面临“意识上传”伦理争议,多国启动立法前瞻研究。
医保支付改革倒逼创新:按疾病诊断相关分组(DRG)与按疗效付费(VBP)模式推广,促使企业从“销售导向”转向“价值导向”,高临床价值药物获得溢价空间。
4. 市场需求:健康消费升级与未满足需求并存
老龄化驱动慢性病管理需求:全球60岁以上人口占比突破,阿尔茨海默病、心血管疾病等年龄相关疾病药物市场持续增长;居家护理机器人、可穿戴监测设备成为银发经济新增长点。
肿瘤成为最大医疗支出领域:免疫治疗、靶向治疗等创新疗法普及,但高昂费用引发公平性争议;液体活检技术通过循环肿瘤DNA(ctDNA)检测实现早筛普惠,市场渗透率快速提升。
罕见病治疗从“孤儿”到“蓝海”:全球已知罕见病超7000种,患者总数超3亿;基因疗法、反义寡核苷酸(ASO)药物为脊髓性肌萎缩症(SMA)、杜氏肌营养不良症等提供根治可能,但支付难题仍待解决。
二、发展趋势:五大维度重塑行业未来
据中研普华产业研究院的《2026-2030年生物医药行业并购重组机会及投融资战略研究咨询报告》分析
1. 技术前沿:从“工具创新”到“范式革命”
多组学整合驱动精准医疗:基因组、蛋白质组、代谢组数据融合,结合单细胞测序与空间转录组技术,实现疾病分型从“组织水平”到“细胞水平”的跨越;微生物组研究揭示肠道菌群与抑郁症、自身免疫病的关联,催生“菌群移植”新疗法。
类器官与器官芯片替代动物实验:3D生物打印技术构建心肌类器官、肝芯片等模型,显著提高药物毒性测试准确性;患者来源类器官(PDO)用于个体化用药预测,降低临床试验失败率。
量子计算破解生物复杂系统:量子算法模拟蛋白质折叠、酶催化反应等过程,解决经典计算机难以处理的分子动力学问题;量子传感器实现单分子水平生物信号检测,推动早诊技术突破。
2. 产业变革:从“线性创新”到“生态竞争”
开放式创新成为主流:药企通过“风险共担、收益共享”模式与初创公司合作;开源药物发现平台(如Atomwise、BenchSci)降低研发门槛,形成“众包创新”生态。
生物制造颠覆传统化工:合成生物学技术生产蜘蛛丝蛋白、生物塑料等材料,替代石油基产品;细胞培养肉技术通过无血清培养基实现规模化生产,缓解粮食安全与环境污染压力。
数据资产成为核心竞争要素:医疗大数据平台整合电子病历、基因组、可穿戴设备数据,构建“数字孪生”模型;区块链技术确保数据溯源与隐私保护,激活沉睡数据价值。
3. 政策导向:从“被动应对”到“主动治理”
全球卫生治理体系重构:WHO推动《大流行病预防、准备和应对公约》落地,建立疫苗、药物公平分配机制;各国加强生物安全立法,防范基因驱动技术、合成病原体的滥用风险。
碳中和目标倒逼绿色转型:生物医药行业纳入碳交易市场,企业通过可再生能源供电、废弃物循环利用降低碳足迹;绿色化学工艺替代有机溶剂,减少药物生产污染。
发展中国家崛起改变产业格局:印度通过专利强制许可制度提升仿制药可及性;巴西、南非等国依托本土生物多样性开发天然药物,形成差异化竞争优势。
4. 市场需求:从“治疗疾病”到“促进健康”
预防医学成为主流:基因检测普及使遗传病风险评估前置;肠道菌群调节、抗氧化补充剂等“营养基因组学”产品市场快速增长;抗衰老研究从延长寿命转向提升健康寿命(Healthspan)。
消费级生物科技兴起:家用基因检测盒、智能药盒、AI皮肤分析仪等产品满足个性化健康管理需求;生物黑客(Biohacker)群体通过DIY基因编辑、神经反馈训练探索人体潜能,引发监管关注。
全球健康不平等加剧:高收入国家占据创新药物90%市场份额,低收入国家仍面临疫苗短缺、基本药物可及性低等问题;国际组织推动“全球公共产品”模式,促进技术转让与能力建设。
5. 伦理与社会:从“技术争议”到“文明对话”
人类增强技术引发身份认同危机:脑机接口实现记忆存储与共享,基因编辑提升认知能力,挑战“人类本质”定义;各国启动“后人类主义”哲学研究,构建技术使用的伦理框架。
生物艺术拓展认知边界:艺术家利用CRISPR技术创作“活体雕塑”,通过微生物发光表达生态警示;生物艺术展览成为公众理解生命科学的新场景,推动科学传播模式创新。
传统医学与现代生物技术融合:青蒿素、三氧化二砷(砒霜)等传统药物成分通过机制研究获得国际认可;针灸、瑜伽等非药物疗法与神经科学结合,形成整合医学新范式。
三、挑战与应对:构建可持续创新生态
1. 技术风险:安全性与可控性
基因驱动技术:可能通过生态系统扩散引发不可逆影响,需建立地理隔离与分子开关控制机制。
AI黑箱问题:深度学习模型决策过程不透明,可能加剧医疗偏见,需开发可解释性算法与伦理审查工具。
2. 产业瓶颈:成本与可及性
CAR-T疗法:单次治疗费用超数十万美元,需通过自动化生产、通用型CAR-T降低成本。
罕见病药物:患者群体小导致研发回报低,需探索“孤儿药共享平台”与“优先审评+市场独占期”激励政策。
3. 社会争议:公平与隐私
基因数据滥用:雇主、保险公司可能基于基因信息歧视个体,需立法禁止基因歧视并建立数据匿名化标准。
生物样本所有权:患者对自身组织、细胞的所有权界定模糊,需明确知情同意与利益分享机制。
2026年的生物医药行业,正站在“治愈疾病”与“重塑人类”的历史交汇点。技术突破带来前所未有的希望,也引发深刻的伦理、社会与治理挑战。唯有坚持“以人为本”的创新导向,构建政府、企业、科研机构、公众多方协同的治理体系,才能确保生物科技真正服务于全人类健康福祉。未来十年,生物医药不仅是经济增长的引擎,更将成为推动文明进步的核心力量——从延长寿命到提升生命质量,从治疗疾病到预防健康,从人类中心到生态共生,一场关于生命的革命正在悄然发生。
欲获取更多行业市场数据及报告专业解析,可以点击查看中研普华产业研究院的《2026-2030年生物医药行业并购重组机会及投融资战略研究咨询报告》。





















 研究院服务号
研究院服务号
 中研网订阅号
中研网订阅号